Posologies initiales (1)
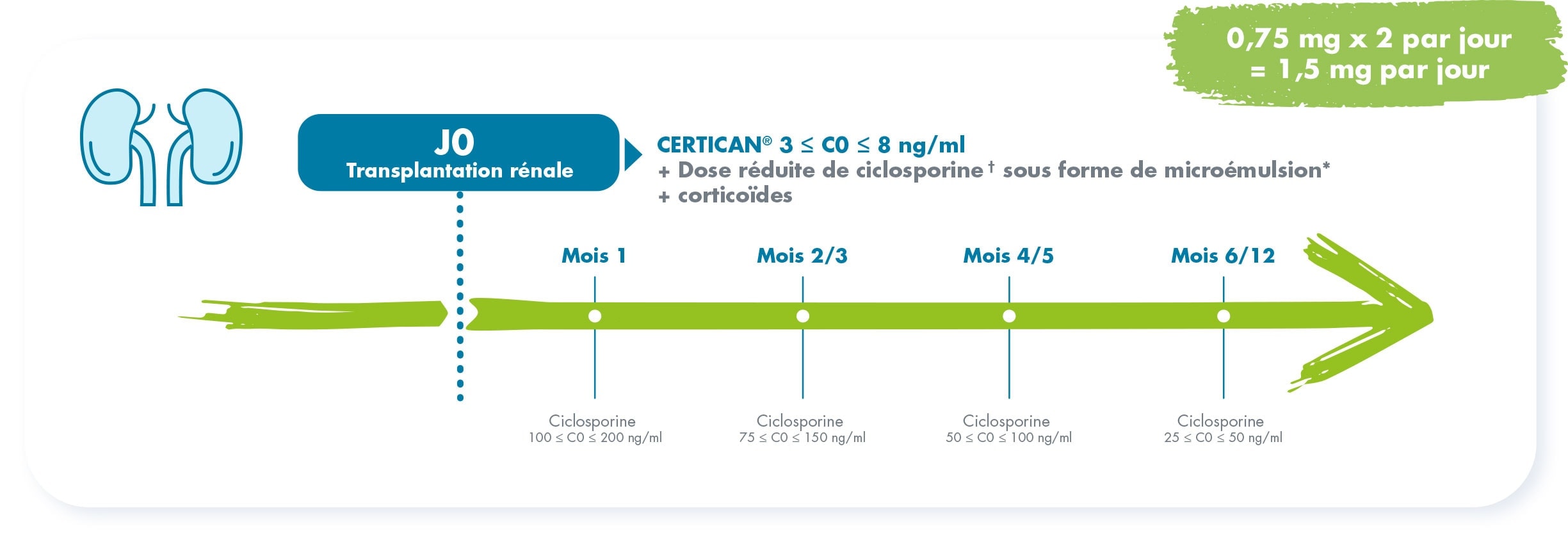
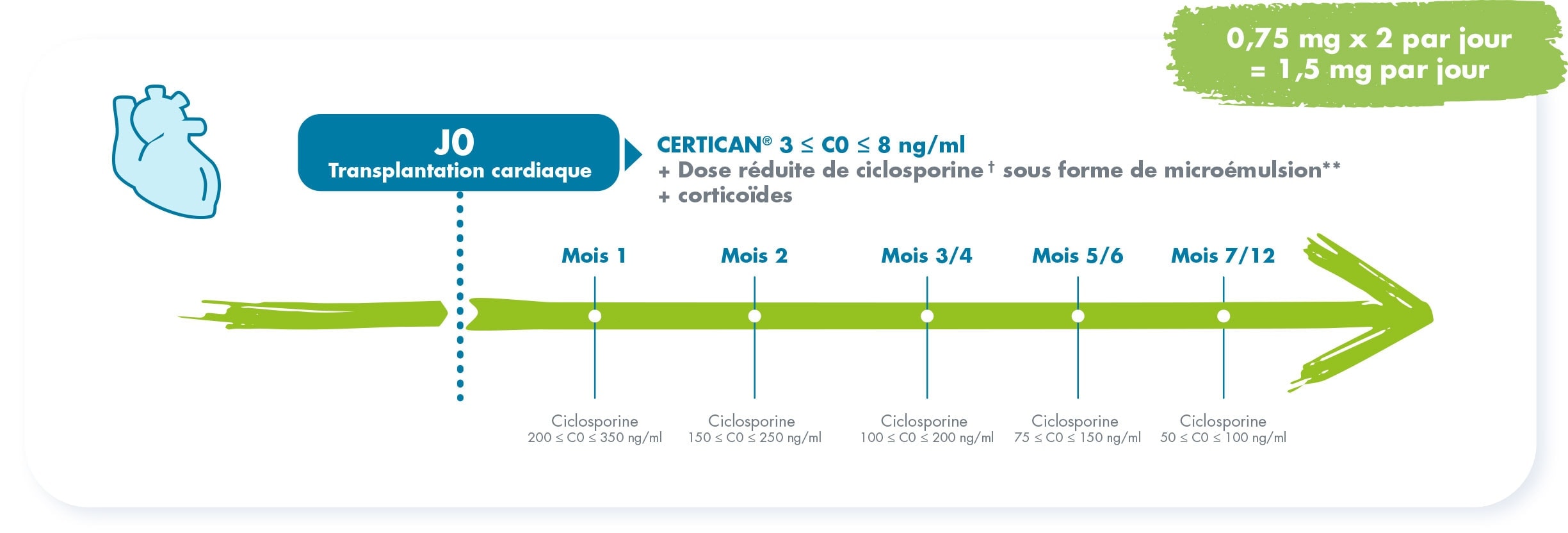
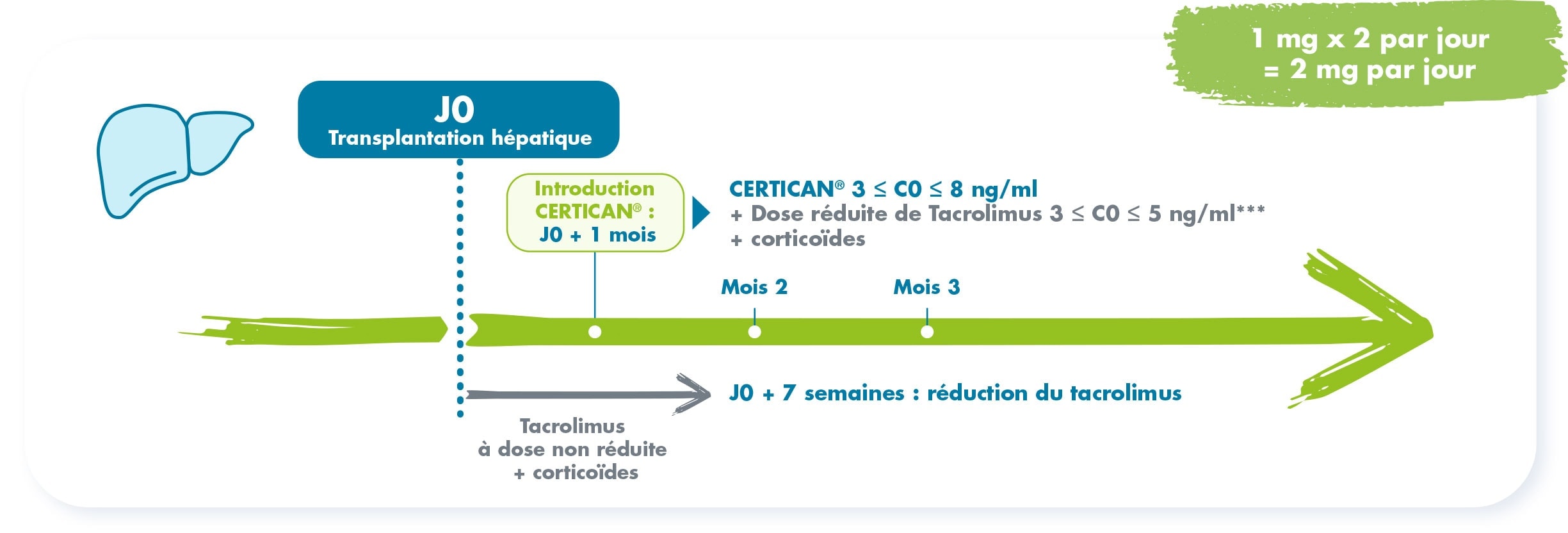
Adaptations posologiques (1)
- Une surveillance régulière des concentrations de l‘évérolimus dans le sang total est recommandée. CERTICAN® a une marge thérapeutique étroite, ce qui peut nécessiter des ajustements de la posologie pour maintenir les réponses thérapeutiques.
- L’utilisation de techniques de dosage ayant des caractéristiques de performance adéquates pour de faibles concentrations de ciclosporine ou de tacrolimus est recommandée
- Ajustements de posologie peuvent être réalisés à 4-5 jours d’intervalle.
- Adaptations posologiques en fonction : des concentrations sanguines atteintes, de la tolérance, de la réponse individuelle, d’une modification des médicaments associés, de la situation clinique.
- Des adaptations posologiques sont nécessaires pour les insuffisants hépatiques.
- Pour plus d’information sur les populations particulières (patients > 65 ans, patients de race noire et population pédiatrique), se reporter au Résumé des Caractéristiques du Produit CERTICAN®.
† La ciclosporine est indiquée dans les greffes d’organe et de tissus. Prévention du rejet du greffon, y compris dans la phase initiale de la transplantation hépatique. Traitement du rejet, chez les patients initialement traités par d’autres protocoles immunosuppresseurs (pour éviter les risques associés à une immunodépression trop forte).
* CERTICAN® ne doit pas être utilisé au long cours avec des doses standard de ciclosporine. Chez les patients transplantés rénaux traités par CERTICAN®, une exposition réduite à la ciclosporine améliore la fonction rénale. Sur la base des données de l’étude A2309, la réduction de l’exposition à la ciclosporine doit être débutée immédiatement après la transplantation avec des concentrations résiduelles dans le sang total comprises dans les fourchettes recommandées. Avant toute réduction de dose de ciclosporine, il convient de s’assurer que les concentrations résiduelles de l’évérolimus dans le sang total à l’état d’équilibre sont supérieures ou égales à 3 ng/ml. Les données relatives à l’administration de CERTICAN® en traitement d’entretien avec des concentrations résiduelles de ciclosporine inférieures à 50 ng/ml ou des valeurs de C2 inférieures à 350 ng/ml sont limitées. Au cas où une réduction de l’exposition à la ciclosporine ne peut être envisagée, la poursuite de l’utilisation de CERTICAN® doit être reconsidérée.
** Chez les patients transplantés cardiaques en traitement d’entretien, la dose de ciclosporine doit être réduite autant que cela est cliniquement possible, afin d’améliorer la fonction rénale. En cas de détérioration progressive de la fonction rénale ou de valeur calculée de la clairance de la créatinine < 60 ml/min, le traitement devra être ajusté. Chez les patients transplantés cardiaques, la dose de ciclosporine peut être établie sur la base des valeurs des concentrations résiduelles de ciclosporine dans le sang. Les données relatives à l’administration de CERTICAN® avec des concentrations résiduelles de ciclosporine de 50 à 100 ng/ml après 12 mois sont limitées en transplantation cardiaque. Avant toute réduction de la dose de ciclosporine, il convient de s’assurer que les concentrations résiduelles de l’évérolimus dans le sang total à l’état d’équilibre sont supérieures ou égales à 3 ng/ml.
*** Chez les patients transplantés hépatiques, l’exposition au tacrolimus doit être réduite afin de minimiser la toxicité rénale liée à l’inhibiteur de la calcineurine. La réduction de la dose de tacrolimus doit être initiée environ 3 semaines après le début de l’association avec CERTICAN® et doit être établie sur la base de concentrations sanguines résiduelles cibles de tacrolimus (C0) comprises dans l’intervalle 3-5 ng/ml. Dans un essai clinique contrôlé, l’arrêt total du tacrolimus a été associé à un risque accru de rejets aigus. Dans les essais cliniques contrôlés, CERTICAN® n’a pas été évalué avec des doses standard (non réduites) de tacrolimus.
(1) Résumé des Caractéristiques du Produit CERTICAN®.

